Ведение пациентов с массивной, субмассивной тромбоэмболией легочной артерии, илеофеморальным тромбозом глубоких вен и хронической тромбоэмболической легочной гипертензией.
A Scientific Statement From the American Heart Association, 2011.
1. Определения
А. Массивная тромбоэмболия легочной артерии (ТЭЛА): острая ТЭЛА с а) устойчивой гипотонией (систолическое АД (САД) < 90 мм рт.ст. в течение как минимум 15 минут, или потребность в инотропной поддержке) по причинам, которые не могут быть обусловлены иной патологией, кроме ТЭЛА (аритмии, гиповолемия, сепсис, дисфунция ЛЖ),
б) отсутствием пульса или
в) персистирующей значимой брадикардией (ЧСС < 40 уд/мин или признаки шока).
Б. Субмассивная ТЭЛА: острая ТЭЛА без системной гипотонии (САД≥90 мм рт.ст.), но с признаками дисфункции правого желудочка (ПЖ) или некроза миокарда.
Дисфункция ПЖ диагностируется на основании одного из следующих признаков:
- дилатация ПЖ (соотношение диаметра ПЖ к диаметру ЛЖ в апикальной четырехкамерной позиции >0,9) или систолическая дисфункция ПЖ по данным ЭХОКГ
- дилатация ПЖ (соотношение диаметра ПЖ к диаметру ЛЖ в четырехкамерной проекции >0,9) по данным КТ
- повышение концентрации BNP > 90 пг/мл
- повышение концентрации N-концевого pro-BNP > 500 пг/мл
- электрокардиографические изменения (вновь диагностированная полная или неполная блокада правой ножки пучка Гиса), передне-перегородочная элевация или депрессия сегмента ST (отведения V1-V4), либо инверсия зубца Т в тех же отведениях
Некроз миокарда диагностируется на основании:
- повышения уровня тропонина I > 0,4 нг/мл или
- повышения уровня тропонина T > 0,1 нг/мл
В. ТЭЛА низкого риска: острая ТЭЛА в отсутствие признаков массивной или субмассивной ТЭЛА.
2. Лечение при массивной, субмассивной ТЭЛА и ТЭЛА низкого риска.
А. Стартовая антикоагулянтная терапия при острой ТЭЛА.
Класс I.
- У пациентов с подтвержденной ТЭЛА и отсутствием противопоказаний к антикоагулянтам должна быть начата антикоагулянтная терапия низкомолекулярными гепаринами (НМГ) подкожно, нефракционированым гепарином (НФГ) внутривенно или подкожно с использованием лабораторного контроля, НФГ подкожно с расчетом дозы по весу пациента без лабораторного контроля либо фондапаринуксом подкожно (уровень доказанности А).
- У пациентов с высокой или промежуточной вероятностью ТЭЛА и отсутствием противопоказаний к антикогулянтам должна быть начата антикоагулянтная терапия в процессе диагностического поиска (уровень доказанности С).
Б. Тромболизис.
Класс IIa.
- Тромболизис может быть проведен у пациентов с массивной острой ТЭЛА и приемлемым риском геморрагических осложнений (уровень доказанности В).
Класс IIb.
- Тромболизис может быть обоснован у пациентов с субмассивной острой ТЭЛА в случае высокого риска осложнений (вновь выявленная гемодинамическая нестабильность, нарастающая респираторная недостаточность, тяжелая дисфункция ПЖ, значительный некроз миокарда) и низким риском кровотечений (уровень доказанности С).
Класс III.
- Тромболизис не рекомендован у пациентов с ТЭЛА низкого риска (уровень доказанности В), а также у пациентов с субмассивной острой ТЭЛА с незначительной дисфункцией правого желудочка, немассивным некрозом миокарда или без ухудшения клинического состояния (уровень доказанности В).
- Тромболизис не показан при недифференцированном сердечном аресте (уровень доказанности В).
Противопоказания к тромболизису аналогичны таковым при остром инфаркте миокарда.
Тромболитик рекомендовано вводить через периферический внутривенный катетер. FDA рекомендует использование альтеплазы 100 мг в виде двухчасовой инфузии. На время инфузии томболитика рекомендовано приостановить введение антикоагулянта.
Предпочтительно получить подтверждение диагноза ТЭЛА с помощью визуализирующей методики до начала тромболитической терапии. Если прямая визуализация недоступна или небезопасна по причине нестабильного состояния пациента, может быть применена агрессивная тактика, предполагающая введение тромболитика пациентам с высокой клинической вероятностью ТЭЛА, дисфункцией ПЖ по данным прикроватной ЭХОКГ, а также стойкой гипотонией (САД< 90 мм рт. ст. или потребность в инотропной поддержке).
На рисунке ниже представлен алгоритм принятия решения о целесообразности проведения тромболизиса для лечения острой ТЭЛА:
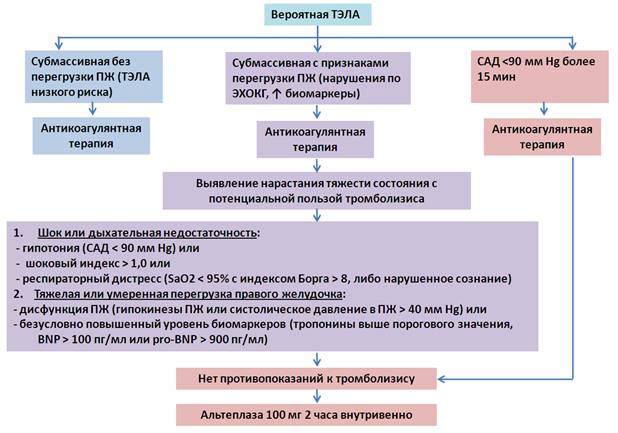
Для выявления пула пациентов с субмассивной ТЭЛА, у которых целесообразно проведение тромболизиса, может быть применено 2 критерия:
- Имеющаяся или прогрессирующая циркуляторная или дыхательная недостаточность
- Тяжелое или умеренное повреждение ПЖ
Циркуляторная недостаточность диагностируется на основании гипотонии или шокового индекса (отношения ЧСС в минуту к САД) > 1. Признаками дыхательной недостаточности является гипоксемия (SaO2 < 95% по данным пульсоксиметрии при дыхании атмосферным воздухом) и клинические проявления респираторного дистресса. Респираторный дистресс также может быть диагностирован по значению индекса Borg, который характеризует степень одышки (0=отсутсвие одышки, 10=удушье). Примерно у 10% пациентов на момент постановки диагноза острой ТЭЛА индекс Borg > 8.
Тяжелое или умеренное повреждение ПЖ может быть диагностировано по данным допплер-ЭХОКГ, которая выявляет гипокинезы ПЖ, признак McConell (отчетливый акинез центра свободной стенки ПЖ при нормальной подвижности верхушки), смещение межжелудочовой перегородки, либо повышение систолического давления в ПЖ > 40 мм рт.ст.). Также повреждение ПЖ может верифицировано по повышению концентрации тропонинов и мозговых натрийуретических пептидов).
В. Катетерная эмболэктомия и фрагментация тромба.
Класс IIa.
- У пациентов с массивной ТЭЛА при наличии противопоказаний к тромболизису может быть проведена катетерная эмболэктомия или фрагментация тромбоэмбола, либо хирургическая эмболэктомия в зависимости от опыта конкретного учреждения (уровень доказанности С).
- У пациентов с массивной ТЭЛА с сохраняющимися после тромболизиса признаками нестабильности может быть проведена катетерная эмболэктомия или фрагментация тромбоэмбола, либо хирургическая эмболэктомия (уровень доказанности С).
- Для пациентов с массивной ТЭЛА при наличии противопоказаний к тромболизису или при сохраняющихся после тромболизиса признаках нестабильности целесообразен перевод в медицинские учреждения, в которых может быть выполнена катетерная эмболэктомия или фрагментация тромбоэмбола, либо хирургическая эмболэктомия при условии недоступности данной процедуры локально и возможности безопасной транспортировки (уровень доказанности С).
Класс IIb.
- Катетерная эмболэктомия или фрагментация тромбоэмбола, либо хирургическая эмболэктомия может быть выполнена пациентам с острой субмассивной ТЭЛА при наличии клинических предикторов неблагоприятного прогноза (вновь зарегистрированная гемодинамическая нестабильность, нарастающая дыхательная недостаточность, тяжелая дисфункция ПЖ или массивный некроз миокарда) (уровень доказанности С).
Класс III.
- Катетерная эмболэктомия или хирургическая эмболэктомия не рекомендована пациентам с ТЭЛА низкого риска или острой субмассивной ТЭЛА с незначительной дисфункцией ПЖ, небольшим объемом некроза миокарда и отсутствием ухудшения общего состояния (уровень доказанности С).
Г. Имплантация кава-фильтров при острой ТЭЛА.
Класс I.
- Взрослым пациентам с подтвержденной острой ТЭЛА (или проксимальным тромбозом глубоких вен (ТГВ)) и противопоказаниями к антикоагулянтам, либо с активным кровотечением показана имплантация кава-фильтров (уровень доказанности С).
- У пациентов с установленным кава-фильтром в случае устранения противопоказаний к антикоагулянтам или прекращения активного кровотечения должна быть назначена терапия антикоагулянтами (уровень доказанности В).
- Пациентам с установленным съемным кава-фильтром в течение временного интервала, в котором может функционировать съемный кава-фильтр, периодически необходимо оценивать целесообразность его удаления (уровень доказанности С).
Класс IIa.
- Установка кава-фильтра целесообразна у пациентов с повторными эпизодами острой ТЭЛА несмотря на адекватную антикоагулянтную терапию (уровень доказанности С).
- У пациентов с ТЭЛА или ТГВ и длительными противопоказаниями к антикоагулянтам целесообразна имплантация постоянного кава-фильтра (уровень доказанности С).
- У пациентов с ТЭЛА или ТГВ и краткосрочными противопоказаниями к антикоагулянтам целесообразна имплантация съемного кава-фильтра (уровень доказанности С).
Класс IIb.
- Установка кава-фильтра может быть целесообразна у пациентов с острой ТЭЛА и очень низким кардиопульмональным резервом, включая эпизоды массивной ТЭЛА (уровень доказанности С).
Класс III.
- Кава-фильтры не должны устанавливаться рутинно параллельно с антикоагулянтами или тромболизисом в качестве лечебного мероприятия при острой ТЭЛА (уровень доказанности С).
Д. Парадоксальная эмболия.
Класс IIb.
- Пациентам с массивной и субмассивной ТЭЛА может быть целесообразен скрининг на наличие открытого овального окна с использованием эхокардиографии с контрастированием солевым раствором с пузырьками воздуха, либо с использованием транскраниального допплеровского исследования для стратификации риска осложнений (уровень доказанности С).
- У пациентов с ТЭЛА любого типа и угрожающей парадоксальной эмболией (тромб, пенетрирующий открытое овальное окно) может быть целесообразна хирургическая эмболэктомия (уровень доказанности С).
3. Илиофеморальный тромбоз глубоких вен (ИФТГВ)–
полный или частичный тромбоз любого фрагмента подвздошных вен или общих бедренных вен с или без вовлечения любых других вен нижних конечностей или нижней полой вены. Данная локализация тромбоза связана с бóльшим риском осложнений.
А. Начальная антикоагулянтная терапия при ИФТГВ
Класс I.
- В отсутствие доказанной или предполагаемой гепарин-индуцированной тромбоцитопении пациенты с ИФТГВ должны получать терапевтические дозы НФГ внутривенно (уровень доказанности А), или НФГ подкожно (уровень доказанности В), или НМГ (уровень доказанности А), или фондапаринукс (уровень доказанности А).
- Пациенты с доказанной или предполагаемой гепарин-индуцированной тромбоцитопенией должны получать прямые ингибиторы тромбина (уровень доказанности В).
У взрослых пациентов рекомендован один из следующих режимов антикоагулянтной терапии:
- НФГ внутривенно начиная с болюса в дозе 80 Ед/кг массы тела, далее – инфузия в течение 5-7 суток с начальной скоростью 18 Ед/кг/час с последующей корректировкой дозы для достижения целевого значения АЧТВ (соответствующее уровню гепарина в плазме 0,3-0,7 МЕ/мл анти-Хa активности);
- НМГ подкожно без рутинного контроля анти-Ха активности (эноксапарин 2 раза в день по 1 мг/кг или 1 раз в сутки 1,5 мг/кг; дальтепарин 1 раз в сутки 200 МЕ/кг или дважды в сути по 100 МЕ/кг; тинзапарин один раз в сутки 175 анти-Ха МЕ/кг);
- Фондапаринукс подкожно один раз в день 5 мг для пациентов весом < 50 кг, 7,5 мг для пациентов весом 50-100 кг и 10 мг для пациентов весом > 100 кг.
- Также может быть назначен НФГ подкожно в фиксированной дозе, рассчитанной по весу пациента, однако этот режим дозирования менее изучен.
Данные об амбулаторном использовании парентеральных антикоагулянтов ограничены.
У детей необходимо назначение антикоагулянтов с расчетом дозы по весу с поправкой на возраст.
Б. Длительная антикоагулянтная терапия при ИФТГВ.
Класс I.
- В случае применения варфарина в качестве препарата для длительной антикоагулянтной терапии, он должен использоваться одновременно («перекрещиваться») с препаратом начальной антикоагулянтной терапии как минимум в течении 5 дней до того момента, как МНО составит ≥2 как минимум в течение 24 часов, в дальнейшем оставаясь в целевом диапазоне 2-3 (уровень доказанности А).
- Пациенты с первым эпизодом ИФТГВ, который произошел на фоне большого устранимого фактора риска, должны получать антикоагулянты в течение 3 месяцев (уровень доказанности А).
- Пациенты с повторным эпизодом ИФТГВ, либо с идиопатическим ИФТГВ должны получать антикоагулянты в течение 6 месяцев, а в дальнейшем – постоянно с регулярной оценкой риска/пользы дальнейшего продолжения антикоагулянтной терапии (уровень доказанности А).
- Онкологические пациенты с ИФТГВ должны получать НМГ в виде монотерапии в течение 3-6 месяцев, либо на протяжении того периода времени, пока сохраняется рак или продолжается его лечение (например, химиотерапия) (уровень доказанности А).
Класс IIb.
1. У детей с ТГВ целесообразным может быть использовано НМГ в виде монотерапии (уровень доказанности С).
Рекомендованы следующие режимы монотерапии НМГ у взрослых пациентов с онкологическими заболеваниями:
- Дальтепарин один раз в день подкожно 200 МЕ/кг (макс 18 000 МЕ) в течение первых 4 недель, далее по 150 МЕ/кг.
- Тинзапарин 1 раз в день подкожно 175 анти-Xа Ед/кг.
- Эноксапарин подкожно один раз в день 1,5 мг/кг.
Если по каким-либо причинам проведение монотерапии НМГ невозможно, адекватной альтернативой является применение варфарина с достижением целевого диапазона МНО 2-3.
В. Компрессионная терапия.
Класс I.
- Пациенты, перенесшие ИФТГВ, должны носить компрессионные гольфы (с макс. давлением 30-40 мм рт.ст.) ежедневно в течение как минимум 2 лет после эпизода ТГВ (уровень доказанности В).
Класс IIa.
- Целесообразно ежедневное использование компрессионных гольфов с максимальным давлением 30-40 мм рт.ст. у пациентов с ИФТГВ в анамнезе и симптомами посттромбофлебитического синдрома (уровень доказанности С).
Класс IIb.
- Пациентам с перенесенным ИФТГВ и тяжелым отеком может быть показано проведение ряда процедур секвенциальной пневматической компрессии с последующим ежедневным применением компрессионных гольфов с максимальным давлением 30-40 мм рт.ст. (уровень доказанности В).
Г. Кава-фильтры у пациентов с ИФТГВ.
Класс I.
1. Кава-фильтр должен быть установлен взрослым пациентам с проксимальным ТГВ (или ТЭЛА) в случае противопоказаний к антикоагулянтной терапии (уровень доказанности В).
2. Антикоагулянты по возможности должны быть назначены пациентам с кава-фильтром в случае, если противопоказание уже не актуально, либо если они не назначались в связи с острым кровотечением (уровень доказанности В).
3. Пациентам со съемным кава-фильтром в течение периода времени, когда фильтр может быть удален, необходимо регулярно оценивать целесообразность удаления фильтра (уровень доказанности С).
Класс IIa.
- Установка кава-фильтра целесообразна у пациентов с повторными эпизодами ТЭЛА несмотря на адекватную антикоагулянтную терапию (уровень доказанности С).
- Установка постоянного кава-фильтра целесообразна пациентам с длительными показаниями к имплантации кава-фильтра (например, длительные противопоказания к антикоагулянтам) (уровень доказанности С).
- Установка съемного кава-фильтра целесообразна пациентам с временными показаниями к наличию кава-фильтра (например, временные противопоказания к антикоагулянтам) (уровень доказанности С).
Класс IIb.
- Пациентам с повторными эпизодами ТГВ (без ТЭЛА) может быть целесообразна имплантация кава-фильтра (уровень доказанности С).
Класс III.
- Кава-фильтры не должны использоваться в рутинной терапии ИФТГВ (уровень доказанности В).
Рекомендаций относительно предпочтительной модели кава-фильтра нет. Стоит отметить, что за относительно непродолжительный период использования съемных кава-фильтров было опубликовано довольно много сообщений о миграции этих устройств.
Период, в течение которого съемный кава-фильтр может быть удален, составляет от 3 до 12 месяцев в зависимости от конкретной модели. Для предотвращения неблагоприятных последствий имплантации кава-фильтра съемное устройство должно быть своевременно удалено.
Непосредственно перед удалением устройства должна быть выполнена венография. В случае обнаружения массивного тромбоза кава-фильтра или нижней полой вены ниже места установки фильтра, целесообразно воздержаться от удаления устройства, продолжить антикоагулянтную терапию и через некоторое время повторно оценить возможность удаления фильтра. Нет однозначного мнения, каким образом резидуальный тромбоз бедренных вен должен влиять на решение об удалении кава-фильтра. При принятии такого решения следует учитывать ожидаемую продолжительность жизни пациента, кардиопульмональный статус, а также сопутствующие заболевания.
У детей также отмечается затруднение удаления кава-фильтра в связи с тромбозом. Для предотвращения поздних осложнений вопрос об имплантации кава-фильтра должен быть решен особенно тщательно, устройство должно быть удалено по возможности быстро.
Д. Тромборедуктивные стратегии.
Показано, что быстрый лизис тромба при ТГВ может предотвращать клапанную недостаточность, обструкцию вен, повторные венозные тромбозы и посттромбофлебитический синдром (ПТФС).
Класс I.
- Управляемый (катетер-направленный) тромболизис и фармакомеханический тромболизис может быть использован у пациентов с ИФТГВ при наличии угрожающих конечности нарушений гемодинамики (phlegmasia cerulea dolens) (уровень доказанности С).
- В случае наличия у пациента с ИФТГВ показаний к эндоваскулярному тромболизису и отсутствием такой возможности в данном стационаре должна быть оценена возможность перевода пациента в центр с соответствующими возможностями (уровень доказанности С).
Класс IIa.
- Управляемый тромболизис или фармакомеханический тромболизис могут быть целесообразны в случае быстрого нарастания тромбоза несмотря на антикоагулянтную терапию (уровень доказанности С) и/или нарастания симптомов несмотря на антикоагулянтную терапию (уровень доказанности В).
- Управляемый тромболизис или фармакомеханический тромболизис целесообразны в качестве терапии первой линии у отдельной категории пациентов с острым ИФТГВ и низким риском геморрагических осложнений с целью профилактики ПТФС (уровень доказанности В).
Класс IIb.
- Выполнение венозной тромбэктомии опытным сосудистым хирургом может быть применено у пациентов с ИФТГВ (уровень доказанности В).
Класс III.
- Системный тромболизис не должен применяться рутинно у пациентов с ИФТГВ (уровень доказанности А).
- Управляемый тромболизис или фармакомеханический тромболизис не должны выполняться у пациентов с хроническим ТГВ (>21 суток) или у пациентов с высоким риском геморрагических осложнений (уровень доказанности В).
Управляемый (катетер-направленный) тромболизис представляет собой введение тромболитика непосредственно в область венозного тромба через катетер с множественными боковыми отверстиями под рентген-контролем.
Рекомендуемые режимы введения тромболитиков:
- Альтеплаза (rtPA) 0,01 мг/кг/час
- Урокиназа 120 000 – 180 000 Ед/час.
Чрескожная механическая тромбэктомия предполагает удаление тромба с помощью специального катетерного устройства путем фрагментации, мацерации и/или аспирации тромба. Использование таких устройств без сопутствующего тромболизиса может приводить к ТЭЛА.
При комбинации чрескожной катетерной тромбэктомии и катетер-направленного тромболизиса (фармакомеханический тромболизис) отмечается эффективность, сопоставимая с изолированным катетер-направленным тромболизисом при значительно меньшей (на 40-50%) используемой дозе тромболитика и времени его инфузии. Возможно, это обстоятельство может приводить к меньшей частоте геморрагических осложнений.
До и после проведения управляемого тромболизиса или фармакомеханического тромболизиса антикоагулянты должны вводиться в соответствии с рекомендациями, изложенными выше. Во время инфузии тромболитика в процессе управляемого тромболизиса дозу НФГ следует снижать. При любых сопутствующих механических манипуляциях (фармакомеханический тромболизис) следует использовать стандартную дозу НФГ.
Во время проведения управляемого тромболизиса не рекомендована процедура имплантации кава-фильтра. Установка съемного кава-фильтра перед процедурой фармакомеханического тромболизиса и его последующее удаление могут быть целесообразны в некоторых ситуациях.
Е. Чрескожная транслюминальная венозная ангиопластика и стентирование.
Чрескожная транслюминальная венозная ангиопластика и стентирование может быть использована рутинно после эндоваскулярной или хирургической тромбэктомии для коррекции обструктивных поражений и профилактики ретромбоза у пациентов с острым ИФТГВ. В частности, эта методика применяется при стенозе левой общей подвздошной вены в сочетании с левосторонним ИФТГВ (синдром компрессии подвздошной вены, синдром May-Thurner, синдром Cockett).
Класс IIa.
- Целесообразно проведение имплантации стента в подвздошную вену с целью коррекции обструктивного поражения после катетер-направленного тромболизиса, фармакомеханического тромболизиса или хирургического удаления тромба (уровень доказанности С).
- Целесообразно проведение попытки чрескожной транслюминальной ангиопластики изолированного обструктивного поражения общей бедренной вены (уровень доказанности С).
- Целесообразна имплантация стентов в подвздошные вены для уменьшения симптомов ПТФС и заживления венозных язв у пациентов с выраженным ПТФС и обструкцией подвздошных вен (уровень доказанности С).
- После имплантации венозных стентов целесообразно применение антикоагулянтов в той же дозе, той же длительностью, с теми же целевыми значениями МНО, что и без стентов (уровень доказанности С).
Класс IIb.
- После имплантации венозных стентов пациентам, у которых предполагается высокий риск ретромбоза, помимо антикоагулянтной терапии, может быть показано проведение антиагрегантной терапии (уровень доказанности С).*
4. Хроническая тромбоэмболическая легочная гипертензия (ХТЛГ) – синдром, включающий одышку, утомляемость, непереносимость физической нагрузки, обусловленные проксимальной тромбоэмболической обструкцией и дистальным ремоделированием легочного сосудистого русла, приводящих к повышению давления в легочной артерии и прогрессирующей правожелудочковой (ПЖ) недостаточности.
К основным патогенетическим механизмам развития ХТЛГ относятся эпизоды повторной эмболии, нарастание тромбоза in situ в боковые ветви ЛА, недостаточное растворение первоначального тромба, что приводит к васкулопатии крупных и мелких легочных сосудов. Если исходный тромб при ТЭЛА не растворяется в течение 1-4 недель, эмболический материал прикрепляется к сосудистой стенке.
А. Классификация тромбоэмболической болезни (ТЭБ):
- Тип 1 (около 25% тромбоэмболической легочной гипертензии) – свежий тромб в общей ЛА или долевых артериях.
- Тип 2 (около 40% случаев) – уплотнение и фиброз интимы с/без организации тромботических масс проксимальнее сегментарных артерий. Это может приводить к диссекции легочных артерий с формированием перепонок в главной и долевых артериях.
- Тип 3 (около 30% случаев) - фиброз, расслоение интимы, ее утолщение с/без организации тромботических масс в дистальных отделах сегментарных и субсегментарных артериях. Это наиболее многообещающий с точки зрения хирургической коррекции тип поражения. В начале сосудистой окклюзии не наблюдается. При этом эндартерэктомия должна быть спланирована индивидуально для каждой сегментарной и субсегментарной артерии.
- Тип 4 (менее 5% случаев) – микроскопическая дистальная васкулопатия артериол без визуализирующейся ТЭБ. Вторичный тромбоз может формироваться за счет стаза. Этот тип поражения может формироваться как следствие ТЭЛА за счет высокого давления или скорости потока крови в сосудах, не адаптированных к этому. Также этот тип поражения может формироваться без предшествующей ТЭЛА.
Б. Предрасполагающие к ХТЛГ факторы:
повторные эпизоды ТЭЛА, большой дефект перфузии, молодой возраст, женский пол, расовая принадлежность (японцы), предшествующая спленэктомия, постоянный венозный катетер, сбросы из желудочков в предсердия, хронические воспалительные состояния (включая хронические заболевания кишки и остеомиелит), серповидно-клеточная анемия, врожденный стоматоцитоз, тиреоидная гормон-заместительная терапия, анамнез онкологического заболевания.
Лабораторные предикторы: волчаночный антикоагулянт (у 10% пациентов с ХТГЛ), любые антифосфолипидные антитела (у 20%), повышенный уровень фактора VIII (39%), врожденный дефицит антитромбина III, протеинов С и S, гепарин-индуцированные антитромбоцитарные антитела, повышенная резистентность к фибринолизу, сниженный уровень тромбомодулина.
В. Прогноз, клиническая картина и диагностика ХТГЛ.
Риск смерти по причине правожелудочковой недостаточности у пациентов с не диагностированной или не леченной ХТГЛ зависит от степени легочной гипертензии (порядка 70% при среднем давлении в ЛА (СДЛА) более 40 мм рт.ст., увеличиваясь до 90% при СДЛА более 50 мм рт.ст.).
Симптомы ХТГЛ зачастую бывают неспецифическими. Наиболее часто встречается прогрессирующая одышка при физической нагрузке со снижением толерантности к физической нагрузке. Для появления одышки в покое необходима окклюзия 60-70% циркуляторного легочного русла. При прогрессировании болезни возможно появление таких дополнительных симптомов, как боль в грудной клетке, головокружение, а также синкопальные состояния. Может развиться кровохарканье. В качестве симптомов ПЖ недостаточности могут развиться периферические отеки, ощущение быстрого насыщения, ощущение переполнения или боль в эпигастрии.
Диагностика ХТГЛ предполагает решение 3 вопросов:
- установление наличия и степени тяжести легочной гипертензии, а также сопутствующей кардиальной дисфункции;
- причина ЛГ;
- возможна ли хирургическая коррекция и в какой степени
- Подтверждение легочной гипертензии. По данным катетеризации правых отделов сердца легочное сосудистое сопротивление в покое превышает 3 единицы Вуда, а систолической и среднее давление в ЛА в покое превышает, соответственно, 40 и 25 мм рт.ст. ЭХОКГ может быть использована только для скрининга, но не для подтверждения диагноза.
- Ангиопульмонография или вентилляционно-перфузионная сцинтиграфия подтверждает обструкцию главной, долевой, сегментарной или субсегментарной легочной артерии несмотря на 3 месяца антикоагулянтной терапии. Нормальные результаты ангиографии или перфузионно-вентилляционной сцинтиграфии исключает диагноз. Важно, что при изменениях по данным сцинтиграфии может наблюдаться практически нормальная картина по данным МСКТ.
- Должны быть исключены другие причины легочной гипертензии (обусловленная патологией ЛЖ и паренхиматозными заболеваниями легких). Для исключения ЛЖ недостаточности, как правило, давление заклинивания легочных капилляров должно быть менее 15 мм рт.ст. У некоторых пациентов давление заклинивания может быть выше по причине выраженной дилатации ПЖ и результирующей диастолической дисфункции ЛЖ. В этом случае отмечается повышение легочного сосудистого сопротивления более 600 дин∙сек∙см-5.
Класс I.
- Пациенты с одышкой, непереносимостью физической нагрузки неизвестной этиологии или признаками ПЖ недостаточности должны быть обследованы на наличие ХТЛГ (уровень доказанности С).
Класс IIa.
- Через 6 недель после перенесенной ТЭЛА целесообразно всем пациентам выполнять ЭХОКГ с целью скрининга на наличие сохраняющейся легочной гипертензии, что может предотвратить развитие ХТГЛ (уровень доказанности С).
Г. Лечение ХТГЛ.
Легочная эндартерэктомия.
После успешного проведения легочной эндартерэктомии отмечается нормализация давления и сопротивления в легочной артерии, что сопровождается повышением сердечного выброса. Как правило, эти эффекты развиваются сразу после операции и достаточно устойчивы.
Согласно публикациям последних трех лет смертность во время процедуры составляет порядка 2,5%.
В послеоперационном периоде наблюдается регресс гипертрофии и дилатации правых отделов, нормализация функции трикуспидального клапана. Через год после успешной операции НК у большинства пациентов не тяжелее I-II ФК.
Послеоперационные осложнения: тяжелое реперфузионное повреждение, манифестирующее в качестве отека легких, является наиболее частым осложнением (5-15% пациентов). В большинстве случаев после короткого периода вентиляционной поддержки и агрессивной диуретической терапии это осложнение разрешается. Легочное кровотечение после этого вмешательства развивается редко.
Отдаленный прогноз: выживаемость в течение 6 лет после операции легочной эндартерэктомии составляет 75-92,3% (по разным источникам). У 62% из ранее признаваемых инвалидами возвращается трудоспособность.
Степень повышения легочного сосудистого сопротивления и возможность его нормализации во время операции – наиболее важный предиктор успешности эндартерэктомии. Размер ПЖ и его функция имеют меньшее значение – т.н. «точки невозврата» в размерах ПЖ, более которых нецелесообразно проводить операцию, не существует. Авторы многократно подчеркивают, что нет верхнего предела легочного сосудистого сопротивления, размеров и функции ПЖ, а также степени трикуспидальной регургитации, которые являлись бы противопоказаниями к операции.
Большие ретроспективные исследования показали, что степень коррекции функции ПЖ и снижения легочной гипертензии зависит от типа тромбоэмболической болезни (см. классификацию выше). Значительно лучше исходы после эндартерэктомии у пациентов с 1 и 2 типами болезни. Напротив, пациенты с 3 и 4 типами (значительная легочная гипертензия с незначительной визуализирующейся степенью тромбоэмболии) являются сомнительными кандидатами для хирургического лечения.
Такие параметры, как возраст старше 80 лет, почечная недостаточность и печеночная дисфункция также не являются противопоказаниями к легочной эндартерэктомии, однако увеличивают риск вмешательства.
Противопоказанием является сопутствующее тяжелое поражение паренхимы легких, поскольку улучшение легочной гемодинамики не улучшит симптомов и не замедлит прогрессирования заболевания.
Стандартная терапия варфарином (МНО 2-3) должна проводится до вмешательства и после него пожизненно.
Медикаментозная терапия.
Единственным многоцентровым рандомизированным исследованием медикаментозной терапии, используемой при легочной артериальной гипертензии, для лечения пациентов с ХТГЛ является BENEFiT, в котором исследовалось применение бозентана у неоперабельных пациентов или в случае резидуальной болезни после операции. Через 16 нед терапии отмечалось небольшое снижение легочного сосудистого сопротивления при отсутсвии улучшения клинической картины.
Класс I.
- У пациентов с объективно доказанной ХТГЛ должна быть незамедлительно оценена возможность проведения легочной эндартерэктомии, даже если симптомы незначительные (уровень доказанности В).
- Пациенты с доказанной ХТГЛ должны получать постоянную антикоагулянтную терапию в случае отсутствия противопоказаний (уровень доказанности С).
Класс IIb.
- Медикаментозная терапия, используемая при артериальной легочной гипертензии (I тип по классификации WHO) может быть целесообразна у пациентов, которые не являются кандидатами на проведение хирургического лечения (вследствие сопутствующей патологии или отказа пациента), либо у которых присутствует резидуальная легочная гипертензия в послеоперационном периоде и им не возможно выполнение повторного вмешательства в медицинском центре с соответствующим опытом (уровень доказанности В).
Класс III.
- Медикаментозная терапия, используемая при артериальной легочной гипертензии (I тип по классификации WHO), не может быть применена вместо легочной эндартерэктомии у пациентов с объективно доказанной ХТГЛ, если они являются или могут быть кандидатами для хирургического лечения в медицинском центре с соответствующим опытом (уровень доказанности В).
По материалам Management of Massive and Submassive Pulmonary Embolism, Iliofemoral Deep Vein Thrombosis, and Chronic Thromboembolic Pulmonary Hypertension. Michael R. Jaff, M. Sean McMurtry, Stephen L. Archer et al. Circulation. 2011;123:00-00.
