Влияние сопутствующего приема ингибиторов протонного насоса на эффективность клопидогрела в исследованиях CAPRIE и CREDO. Мета-анализ исследований CAPRIE, CREDO, TRITON и PLATO.
Предпосылки:
Клопидогрел в комбинации с аспирином является основой профилактики инфаркта миокарда (ИМ) и тромбоза стентов после острого коронарного синдрома (ОКС) и чрескожного коронарного вмешательства (ЧКВ). Клопидогрел является пролекарством, для образования активного метаболита которого требуется участие системы цитохрома (CYP) Р450 (изоферментов СYP3A4, CYP1A2, CYP2C9, CYP2C19 и/или СYP2B6). Такой путь метаболизма клопидогрела породил ряд теоретических рассуждений о потенциальном влиянии на его эффективность препаратов, усиливающих или ослабляющих активность перечисленных изоферментов системы CYP 450, особенно CYP2C19. Ряд исследований подтвердил наличие такого влияния на ингибирование клопидогрелом реактивности тромбоцитов ex vivo, однако получить доказательства значимого клинического эффекта оказалось значительно труднее.
Важным представляется идентификация такого влияния ингибиторов протонного насоса (ИПН), многие из которых ингибируют CYP2C19, поскольку они рекомендованы как препараты первой линии для профилактики желудочно-кишечных осложнений у пациентов высокого риска. Клопидогрел и ИПН входят в перечень наиболее назначаемых во всем мире лекарственных препаратов, и, соответственно, часто принимаются совместно.
Впервые на возможность взаимодействия между клопидогрелом и ИПН указали Gilard и соавторы, продемонстрировавшие повышенную реактивность тромбоцитов на фоне клопидогрела в случае сопутствующего применения ИПН у пациентов после ЧКВ. Клинический эффект (повышение частоты неблагоприятных событий на фоне совместного приема клопидогрела и ИПН) был продемонстрирован, в основном, в обсервационных исследованиях и регистрах (во многих, но не во всех), тогда как анализ рандомизированных клинических испытаний продемонстрировал отсутствие значимого клинического взаимодействия. Клиническая значимость этого взаимодействия продолжает обсуждаться. Так, FDA и European Medicines Agency не рекомендуют использовать одновременно с ИПН клопидогрел и ингибиторы CYP2C19, специально подчеркивая эту рекомендацию для омепразола и эзомепразола.
Задачей авторов данной статьи была оценка влияния ИПН на эффективность клопидогрела по данным 2 крупных плацебо-контролируемых исследований, в которых прием ИПН был документирован: CREDO («клопидогрел для профилактики неблагоприятных событий за время наблюдения») и СAPRIE («клопидогрел против аспирина у пациентов с риском ишемических событий»).
Методы:
Данное исследование представляет собой ретроспективный post hoc анализ ранее опубликованных результатов исследований CAPRIE и CREDO.
Исследование CREDO: проспективное рандомизированное двойное слепое плацебо-контролируемое, включившее 2116 пациентов (1999-2001гг). Пациенты рандомизировались через 3-24 часа после ЧКВ к приему нагрузочной дозы клопидогрела 300 мг или плацебо. В дальнейшем в течение 28 дней все пациенты в открытом режиме получали клопидогрел 75 мг/сут. По прошествии 28 дней пациенты, которые получили нагрузочную дозу клопидогрела, продолжили его прием 75 мг/сут в течение еще 11 месяцев. Пациенты, получившие плацебо при рандомизации, получали плацебо с 29 дня исследования в течение 11 месяцев. Первичная комбинированная конечная точка за 28 сут. состояла из ИМ, экстренной реваскуляризации в целевом сосудистом бассейне и смерти от всех причин; первичная конечная точка за 1 год включила смерть от всех причин, ИМ и инсульт.
Исследование CAPRIE: рандомизированное проспективное; всего было включено 19185 пациентов высокого риска (с перенесенным ранее ИМ, инсультом или периферическим атеросклерозом), которые рандомизировались (1992-1995 гг) к приему в виде монотерапии клопидогрела 75 мг/сут или аспирина 325 мг/сут. Первичная конечная точка была также комбинированной и включала в себя ишемический инсульт, ИМ или смерть от сердечно-сосудистых причин минимум после 1 года лечения.
Также авторами был выполнен мета-анализ, в котором данные из исследований CREDO и СAPRIE были объединены с результатами опубликованных слепых рандомизированных контролируемых исследований, в рамках которых клопидогрел сравнивался с препаратами, теоретически не взаимодействующими с ИПН; еще одним условием отбора исследований является доступность данных по использованию ИПН. Т.о., мета-анализ включил результаты исследований CREDO, CAPRIE, TRITON и PLATO. Целью мета-анализа был расчет скорректированных ОШ первичных конечных точек у пациентов принимающих и не принимающих ИПН, рандомизированных к клопидогрелу или другой терапии. В исследованиях TRITON и PLATO первичная конечна точка состояла из ИМ, инсульта и смерти от сердечно-сосудистых причин. Пациенты в этих исследованиях были рандомизированы к приему клопидогрела либо другого антиагреганта (празугрела и тикагрелора, соответственно).
Применение ИПН.
Решение о назначении ИПН принималось лечащими врачами и не являлось обязательным с точки зрения протокола. Применение ИПН фиксировалось на момент включения пациента в исследование и на каждом визите. Для данного анализа пациенты считались «принимающими» ИПН в случае, если они получали активное лечение этими препаратами (омепразолом, лансопразолом, рабепразолом, пантопразолом или эзомепразолом). Прием ИПН оценивался как время-зависимая коварианта. Если на визите пациент принимал ИПН, то дата старта приема рассчитывалась как 1 день после визита, на котором на вопрос о приеме этого препарата было отвечено отрицательно. Если прием ИПН прекращался, дата приостановки приема рассчитывалась как 1 день после визита, на котором на вопрос о приеме препарата ответ был положительным.
Результаты
CAPRIE
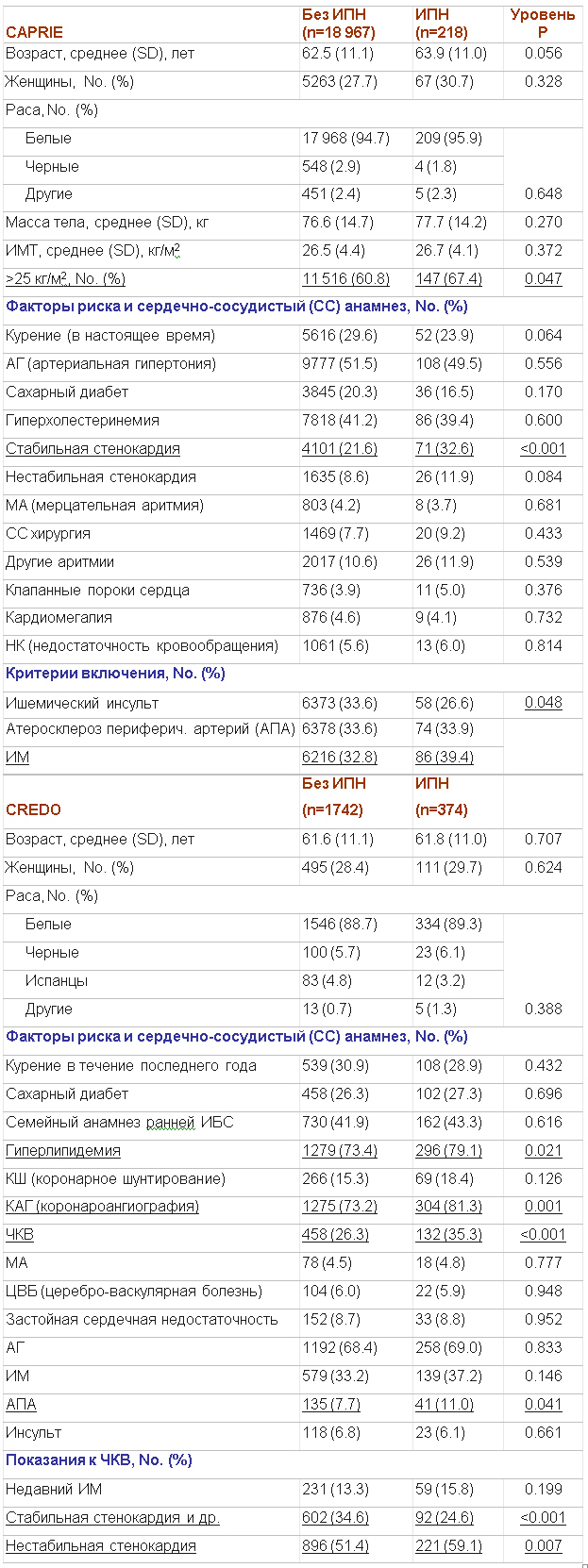
Исходная характеристика пациентов. Из 19185 включенных пациентов 218 (1,1%) получали ИПН в момент включения в исследование. Из них 216 получали омепразол и 2 – лансопразол (оба препарата сильно ингибируют CYP2C19). В таблице 1 приведены исходные характеристики пациентов, разделенных на группы в зависимости от факта приема ИПН. В целом пациенты, получающие ИПН, характеризовались большей частотой ИМТ > 25 кг/м2, у них чаще встречалась стабильная стенокардия. Кроме того, у принимающих ИПН чаще основанием для включения в исследование являлся перенесенный ранее ИМ.
Таблица 1. Исходные характеристики пациентов исследований CAPRIE и CREDO в зависимости от исходного использования ИПН.
Первичная конечная точка.
Частота первичной конечной точки (ИИ, ИМ и СС смерть) у пациентов, принимающих ИПН на момент включения в исследование, составила 11,7% в группе клопидогрела и 4,7% в группе аспирина (нескорректированное вычисленное ОШ 2,66; 95% ДИ 0,94-7,5) (таблица 2). У пациентов, не получающих ИПН в начале исследования, частота первичной конечной точки составила 9,8% в группе клопидогрела против 10,7% в группе аспирина (нескорректированное вычисленное ОШ 0,90; 95% ДИ 0,83-0,99). Т.о., данное взаимодействие оказалось статистически значимым (р=0,047).
Таблица 2. Первичная конечная точка в зависимости от использования ИПН (с использованием различных определений «лечения ИПН») в исследовании CAPRIE.
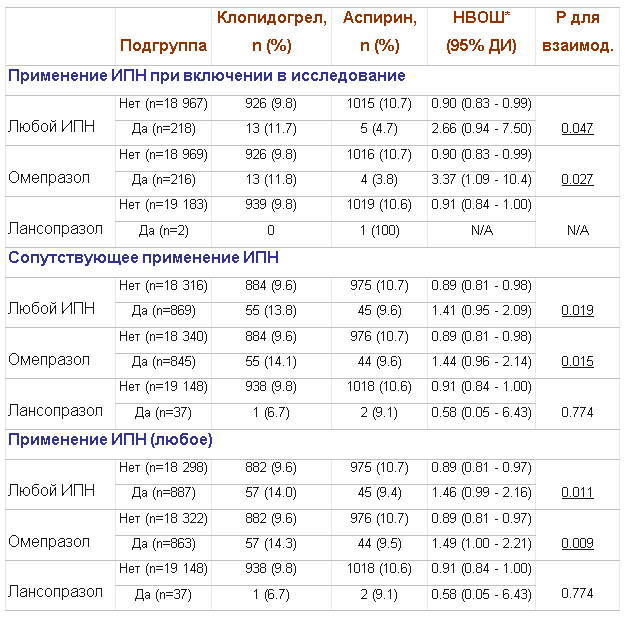
*НВОШ – нескорректированное вычисленное отношение шансов.
У пациентов, рандомизированных к приему клопидогрела (n=9599), частота первичной конечной точки в случае сопутствующего приема ИПН составила 14,0%, без ИПН – 9,6% (НВ ОШ на основе время-зависимой коварианты 2,66; 95% ДИ 1,94-3,63, р<0,001) (таблица 3). у пациентов, рандомизированных к приему аспирина, частота первичной конечной точки на фоне приема ИПН составила 9,4% против 10,7% без ИПН (НВ ОШ 1,17; 95% ДИ 0,78-1,76, р=0,439). После поправки на коварианты, перечисленные в легенде к таблице 3, и стратификации по индексам соответствия ИПН влияние ИПН на эффективность клопидогрела оставалось значимым: скорректированное вычисленное (СВ) ОШ составило 2,39 (95% ДИ 1,74-3,28, р<0,001), р (взаимод.)=0,001. В группе аспирина прием ИПН не влиял на частоту первичной конечной точки: СВ ОШ 1,04 (95% ДИ 0,70-1,57, р=0,834).
Таблица 3. Нескорректированное и скорректированное* вычисленное ОШ (95% ДИ) частоты первичной конечной точки в зависимости от приема ИПН (как время-зависимой коварианты) по результатам исследования CAPRIE.
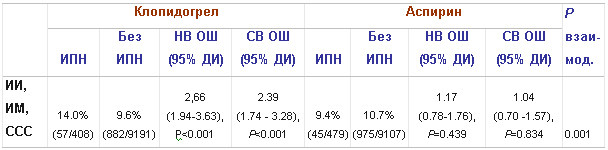
* - скорректированная модель включала такие параметры, как раса, СД, гиперхолестеринемия, ЗСН, кардиомегалия, МА, стабильная стенокардия, НС, предшествующий ИМ, ТИА, обратимый ишемический неврологический дефицит, предшествующий ИИ, перемежающаяся хромота, ампутация нижней конечности.
Также авторами был проведен дополнительный анализ с учетом различных определений приема ИПН. Среди пациентов, которые не принимали ИПН вообще в течение всего исследования клопидогрел оказался на 11% эффективнее аспирина в отношении предотвращения первичной конечной точки; в случае сопутствующего приема ИПН в любой момент исследования частота первичной конечной точки была выше на 46% у принимающих клопидогрел, р взаимод.=0,011 (таблица 2). После коррекции на значимые факторы и стратификации по индексам соответствия прием ИПН в любое время в течение исследования значимо ассоциировалось с увеличением частоты первичной конечной точки в группе клопидогрела (СВ ОШ 1,34; 95% ДИ 1,02-1,76, р=0,033), но не в группе аспирина (СВ ОШ 0,81; 95% ДИ 0,60-1,09, р=0,157).
CREDO
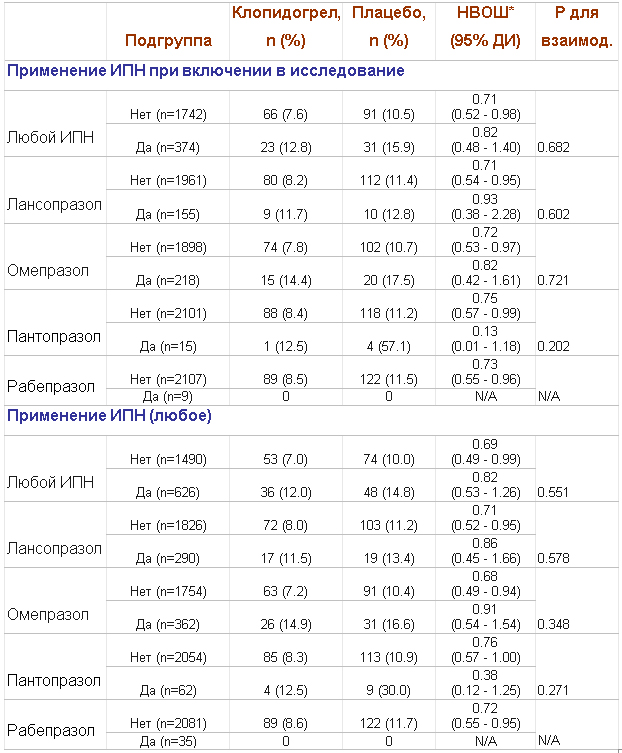
Исходная характеристика пациентов. Из 2116 пациентов, включенных в исследование CREDO, 374 (17,7%) принимали ИПН в момент начала исследования, что значительно превышало данный показатель в популяции CAPRIE. Большинство пациентов получали лансопразол (n=218), реже назначались омепразол (n=155), пантопразол (n=15) и рабепразол (n=9); 23 пациента получали ≥ ИПН в течение исследования. В таблице 1 приведены основные исходные характеристики пациентов. Следует отметить, что у пациентов, получающих ИПН, чаще встречалась гиперлипидемия, ЧКВ и КАГ в анамнезе, атеросклероз периферических артерий. На момент включения в исследование у принимающих ИПН чаще отмечалась НС.
Первичная конечная точка.
Среди пациентов, получающих ИПН на момент включения в исследование, частота первичной конечной точки за 28 сут (смерть от всех причин, ИМ, экстренная реваскуляризация целевого сосуда) в группе клопидогрела составила 11,1%, в группе плацебо 10,3% (НВ ОШ 1,1; 95% ДИ 0,57-2,11) (таблица 4). У пациентов, не получающих ИПН (n=1479), частота первичной конечной точки в группе клопидогрела была 5,8%, в группе плацебо 7,8% (НВ ОШ 0,74; 95% ДИ 0,50-1,10). Т.о., значимого взаимодействия выявить не удалось (р=0,315) (таблица 4).
Таблица 4. Первичная конечная точка (28 сут) в зависимости от использования ИПН (с использованием различных определений «лечения ИПН») в исследовании CREDO.
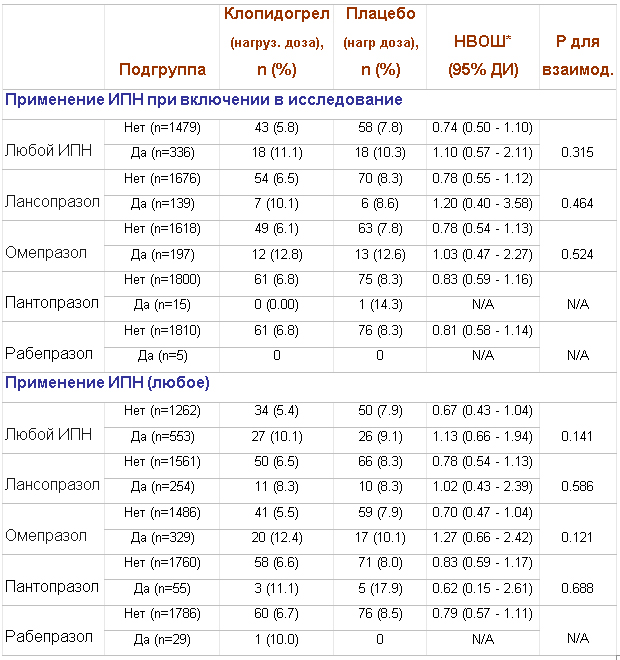
В подгруппе пациентов, рандомизированных к приему нагрузочной дозы клопидогрела (n=900), частота первичной конечной точки через 28 сут у получающих активную терапию ИПН составила 10,1%, у не получающих – 5,4% (НВ ОШ, рассчитанное на основании время-зависимой коварианты, составляет 1,82; 95% ДИ 1,10 -3,04, р=0,021) (таблица 5). У пациентов, рандомизированных к нагрузочной дозе плацебо (n=915) частота первичной конечной точки у получающих активное лечение ИПН составила 9,1% против 7,9% у не получающих ИПН (НВ ОШ 1,16; 95% ДИ 0,72-1,88; р=0,538).
Таблица 5. Нескорректированное и скорректированное* вычисленное ОШ (95% ДИ) частоты первичной конечной точки через 28 сут. в зависимости от приема ИПН (как время-зависимой коварианты) по результатам исследования CREDO.
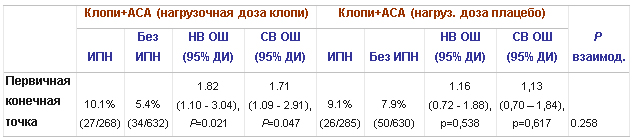
* - скорректированная модель включала такие параметры, как раса, СД, гиперхолестеринемия, ЗСН, МА, стабильная стенокардия, НС, предшествующий ИМ, предшествующий ИИ, АПА, ЧКВ, КАГ, КШ.
После введения поправки на факторы, перечисленные в легенде к таблице 5, а также после стратификации по индексам соответствия ИПН оставались значимым фактором, влияющим на прогноз у пациентов, получивших нагрузочную дозу клопидогрелом (скорректированное вычисленное ОШ, основанное на время-зависимой коварианте, составило 1,71; 95% ДИ 1,09-2,91, р=0,047). У пациентов на плацебо такой зависимости не наблюдалось: СВ ОШ 1,13; 95% ДИ 0,70 – 1,84, р=0,617; р взаимод.=0,258).
Среди пациентов, не получавших ИПН в течение всего времени исследования, риск неблагоприятных событий на фоне приема клопидогрела был на 33% ниже в сравнении с плацебо; у принимающих ИПН риск первичной конечной точки на фоне клопидогрела был на 13% выше, при этом данное взаимодействие не достигало статистической значимости (р=0,141) (таблица 4). После поправки на значимые факторы и стратификации по индексам соответствия любой прием ИПН ассоциировался с увеличением частоты первичной конечной точки через 28 сут. у пациентов, получивших нагрузочную дозу клопидогрела (СВ ОШ 1,81; 95% ДИ 1,07-3,05, р=0,026). у получивших плацебо такой ассоциации выявлено не было: СВ ОШ 1,10; 95% ДИ 0,68-1,79, р=0,692.
Частота первичной конечной точки через год (смерть от всех причин, ИМ, ИИ) у тех пациентов, которые исходно получали ИПН (n=374), составила в группе клопидогрела 12,8%, в группе плацебо 15,9% (НВ ОШ 0,82, 95% ДИ 0,48-1,40) (таблица 6). У пациентов, не получавших ИПН на момент включения в исследование (n=1742), частота первичной конечной точки у принимающих клопидогрел составила 7,6%, у принимавших плацебо – 10,5% (НВ ОШ 0,71, 95% ДИ 0,52-0,98); взаимодействие не было статистически достоверным.
Таблица 6. Первичная конечная точка (1 год) в зависимости от использования ИПН (с использованием различных определений «лечения ИПН») в исследовании CREDO.
У пациентов, рандомизированных к приему клопидогрела (n=1053), частота первичной конечной точки через год на фоне активной терапии ИПН составила 12%, без терапии ИПН – 7% (НВ ОШ, основанное на время-зависимой коварианте, составило 1,68; 95% ДИ 1,07-2,63, р=0,024) (таблица 7). В группе плацебо частота первичной конечной точки на фоне активной терапии ИПН составила 14,8% против 10,0% у не получающих ИПН (НВ ОШ, основанное на время-зависимой коварианте, составило 1,61; 95% ДИ 1,10 – 2,35, р=0,014). После введения поправки на факторы, перечисленные в легенде к таблице 7, а также стратификации по индексам соответствия, прием ИПН продолжал достоверно ассоциироваться с увеличением частоты первичной конечной точки как на фоне терапии клопидогрелом (СВ ОШ 1,67; 95% ДИ 1,06-2,64, р=0,027), так и на фоне плацебо (СВ ОШ 1,56; 95% ДИ 1,06-2,30, р=0,025); р взаимод.=0,811.
Таблица 7. Нескорректированное и скорректированное* вычисленное ОШ (95% ДИ) частоты первичной конечной точки через 1 год в зависимости от приема ИПН (как время-зависимой коварианты) по результатам исследования CREDO.
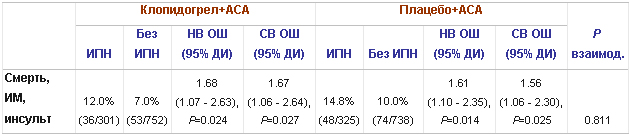
* - скорректированная модель включала такие параметры, как раса, СД, гиперхолестеринемия, ЗСН, МА, стабильная стенокардия, НС, предшествующий ИМ, предшествующий ИИ, АПА, ЧКВ, КАГ, КШ.
Среди пациентов, не получающих ИПН в течение всего исследования, прием клопидогрела снижал частоту конечной точки на 31% в сравнении с принимающими плацебо; в случае приема ИПН в любой период времени в течение исследования эта разница составила лишь 18% (взаимодействие не достигло статистической значимости, р=0,551). После введения поправки на потенциально значимые факторы и стратификации по индексам соответствия прием ИПН ассоциировался с увеличением частоты первичной конечной точки как в группе клопидогрела (СВ ОШ 1,76; 95% ДИ 1,14-2,71, р=0,10), так и в группе плацебо (СВ ОШ 1,49; 95% ДИ 1,03-2,16, р=0,035).
Мета – анализ
В мета-анализ были включены данные, полученные при наблюдении за 53510 пациентами, являющимися участниками четырех рандомизированных контролируемых исследований клопидогрела (26723 пациента рандомизированы к приему клопидогрела, 26787 – к иному антитромбоцитарному препарату, на метаболизм которого ИПН теоретически не влияют). Из числа всех включенных пациентов 12581 получали терапию ИПН (23,5%). Скорректированное рассчитанное отношение шансов среди пациентов на клопидогреле у принимающих ИПН в сравнении с не принимающими составило 1,41 (95% ДИ 0,99-2,00), р=0,053 (рисунок 1). У получающих иную терапию СВ ОШ составило 1,16 (0,98-1,38), р=0,08. Уровень р для взаимодействия между применением ИПН и клопидогрела составило 0,39.
Рисунок 1. Результаты мета-анализа влияния ИПН на частоту первичных конечных точек в рандомизированных контролируемых исследованиях клопидогрела против иной антитромбоцитарной терапии.
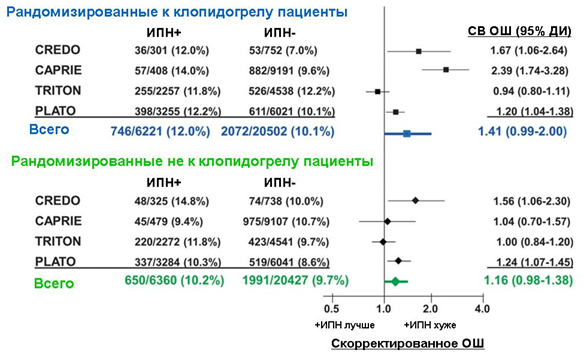
Полученные результаты объясняются тем, что: 1) в исследованиях CREDO и PLATO была продемонстрирована связь между приемом ИПН и частой первичной конечной точки независимо от используемого антиагреганта; 2) в обеих ветвях исследования TRITON сопутствующий прием ИПН не оказывал влияния на частоту неблагоприятных исходов; 3) в исследовании CAPRIE ИПН увеличивали частоту первичной конечной точки у принимающих клопидогрел, но не оказывали влияния на неблагоприятные исходы у принимающих аспирин.
Обсуждение
Результаты исследования CREDO (увеличение частоты неблагоприятных исходов на фоне приема ИПН в обеих группах – клопидогрела и плацебо) во многом созвучны результатам многих опубликованных ранее наблюдательных исследований и анализов различных регистров. Авторы отмечают, что во многих подобных анализах пациенты, получающие ИПН, были старше и тяжелее больных, не получавших такого лечения. В одном из анализов риск тромботических осложнений повышался на фоне совместного приема клопидогрела и всех ИПН (независимо от метаболизма CYP2C19). Blackburn и соавт. показали, что прием препаратов, подавляющих синтез соляной кислоты в желудке (ИПН или гистаминовых блокаторов), ассоциировался с увеличением частоты госпитализаций по поводу ОКС независимо от сопутствующего лечения клопидогрелом.
Исходя из результатов подобных наблюдательных исследований, нельзя исключить прямого кардиотоксического эффекта ИПН. Так, Shillinger и соавт. продемонстрировали снижение сократимости миокарда на фоне приема омепразола и пантопразола. Charlot и соавт. показали, что у пациентов с НК прием ИПН ассоциирован с неблагоприятными СС исходами независимо от сопутствующего лечения клопидогрелом. Bell и соавт. показали, что у пожилых пациентов, помещенных в учреждения закрытого типа, прием ИПН приводит к повышению смерти от всех причин. Schmidt и соавт. продемонстрировали связь между приемом ИПН и неблагоприятными СС исходами после ЧКВ. Самым значимым доказательством против существования прямого кардиотоксического эффекта у ИПН являются, по-видимому, результаты исследования COGENT, в котором все пациенты получали клопидогрел: частота СС событий у рандомизированных к приему ИПН не превышала таковую у принимающих плацебо.
Отдельно стоящие результаты исследования CAPRIE, в котором неблагоприятный эффект ИПН был продемонстрирован только в группе клопидогрела, авторы объясняют следующим образом: возможно, слабое, но достоверное воздействие ИПН на эффективность клопидогрела проявляется именно в той ситуации, когда препарат назначается в качестве монотерапии (в других рандомизированных исследованиях клопидогрел назначался в качестве компонента двойной антитромбоцитарной терапии). Кроме того, подобные результаты могут быть просто случайностью, учитывая недостаточно большое количество пациентов.
В целом авторы заключают, что результаты исследования CREDO подтверждают гипотезу, согласно которой применение ИПН ассоциировано с увеличением частоты неблагоприятных сердечно-сосудистых эпизодов, но не снижает клинической эффективности клопидогрела. Данные выводы подкрепляются результатами выполненного авторами мета-анализа. Тем не менее, результаты исследования CAPRIE указывают на возможное снижение эффективности клопидогрела при сопутствующем приеме ИПН в том случае, если клопидогрел используется в виде монотерапии (без аспирина). Кроме того, результаты этого исследования указывают на необходимость планирования исследований, в котором клопидогрел будет назначаться в виде монотерапии.
По материалам: S.P. Dunn, S. R. Steinhubl, D. Bauer et al. Impact of Proton Pump Inhibitor Therapy on the Efficacy of Clopidogrel in the CAPRIE and CREDO Trials. J Am Heart Assoc. 2013;2:e004564 doi: 10.1161/JAHA.112.004564.
http://jaha.ahajournals.org/content/2/1/e004564.full
